Over tümörlerinden hangisi “psödomiksoma peritonei” oluşumuna en sık neden olur?
A) Seröz tümör
B) Musinöz tümör
C) Endometrioid tümör
D) Berrak hücreli tümör
E) Brenner tümörü
CEVAP: B
————————
Aşağıdaki over tümörlerinden hangisinin ‘‘psödomiksoma peritonei’’ye neden olma olasılığı en yüksektir?
A) Seröz kistadenom
B) Müsinöz tümör**
C) Brenner tümörü
D) Berrak hücreli tümör
E) Endometrioid tümör
—————–
Müsin salgılayan neoplazilerin peritona yaptığı metastaz; Psödomiksoma Peritonei
Overin seröz kist adenokanserinin peritona yaptığı metastaz; Karsinomatozis Peritonei
Overi en çok büyüten tümör;Müsinöz tümör
Müsinöz over tümörleri için risk faktörleri; KRAS mutasyonu ve sigara içimi
Psödomiksoma peritonei‛ye neden olan over tümörü;Müsinöz tümör
Serviks epiteline benzeyen hücreler hangi over tümöründe; Müsinöz tümör
Müsinöz tumor; Overi en çok büyüten tumor olup Psödomiksoma peritonei‛ye neden olan olur, Serviks epiteline benzeyen hücreler görülür.
Musinöz tümörler, tüm over kanserlerinin %10’unu oluştururlar. Bu tümörler histolojik olarak yüksek silendirik epitel hücrelerinin apikal yüzeylerinde vaküollerin varlığı ve sillerin yokluğu ile tanınır. Bu tümörlerin %80’ini kistadenomlar, %10’unu sınır lezyonlar ve kalan %10’unu da kistadenokarsinomlar oluşturur. Musinöz kistadenokarsinomların metastaz ya da rüptürü psödomiksoma peritoneuma yol açar.
Psödomiksoma peritonei (PMP) nadir görülen bir hastalıktır. Her yıl yapılan bir milyon laparotomide bir görülme insidansı bildirilmektedir. Karın içinde müsinöz bir sıvı birikimiyle karakterize inatçı progresif seyirli bir hastalıktır
Bu tabir ilk defa 1884 yılında Werth tarafından kullanılmıştır
1901 yılında Frankel PMP’nin apendiks kisti ile ilişkisini bildirmiştir
PMP’nin etiyolojisini bu tarihlerden itibaren tartışma konusu olmuştur. Orta yaşlarda sık görülür ve kadınlarda erkeklere göre daha sık rastlanır
Olguların çoğu apendiks ve over kaynaklıdır
Hastalığın nadir görülmesi nedeniyle tedavisi de tartışmalıdır
—————————-
“Psödomiksoma peritonei”’nin aşağıdaki organlardan hangisinin tümörlerinden kaynaklanması en az
olasıdır?
A) Over
B) Kolon
C) Dalak*************
D) Pankreas
E) Apendiks
Mukosel; Appendiks lümeninin müsinöz sekresyonu ile dilatasyonudur. Mukozal hiperplazi ile birlikte
müsinöz kistadenoma ya da kistadenokarsinoma vardır.
Müsinöz kistadenoma için apendektomi yapılması yeterlidir.
Kistadenokarsinomlarda, perforasyon veya müsinöz yayılım olmamış ise apendektomi yeterlidir.
Malignansi varlığında geniş cerrahi uygulanır.
Psödomiksoma peritonei varsa kötü prognozu. HİPEC tedavisi (hipertermik intraperitoneal
kemoterapi) ve sitoreduktif cerrahi endikasyonu vardır.
Cevap C
————————-
PMP’nin kaynağı hakkında karışıklık devam etmekteyken bilimsel kanıtlar PMP’nin kaynağının erkeklerde ve kadınlarda daha çok apendiks olduğunu göstermektedir
Kadın hastalarda primer tümör apendikste olmasına rağmen overde büyük bir tümör saptanabilmektedir. PMP hastaları üzerine yapılan çalışmalarda apendiks ve overde kitlesi olan hastalarda, primer kaynağın daha çok apendiks olduğunu göstermiştir
PMP biyolojik olarak agresif bir tümör olarak kabul edilmemektedir. Tümörün periton içi yayılımını tümörün histolojik özellikleri değil karın içi sıvı hidrodinamikleri belirlemektedir[8]. Peritoneal sıvı emiliminin olduğu omentumda tümör implantı daha fazla olurken, peristatizmi olup karın içinde serbest hareket eden ince barsakta implant karın içindeki retroperitona fikse organlara göre daha az olmaktadır. İnvazyon ve lenf nodu metastazı yapmamasına rağmen hastalık ilerleyerek hastanın ölümüne sebeb olmaktadır
Hastaların 5 yıllık ortalama yaşam süreleri %53-75 arasında değişmektedir
PMP genelde apandisit veya karın içi kitle şüphesiyle laparotomi yapılan hastalarda beklenmedik bir durum olarak saptanmaktadır. Görüntüleme yöntemlerinde gelişmeye paralel olarak laparotomiden önce tanı konulan vakalarda artış olmaktadır. Hastalarda tanıda gecikmeye sık rastlanmakta ve tanı konuluncaya kadar bir süre geçmektedir. Şüphelenilen vakalarda ince iğne aspirasyon biyopsileri tanıda yardımcı olabilir, fakat alınan örneklerde hücre sayısı seyrek olduğundan kesin tanı koymak zor olabilir

Tümör markerlerinden CA-125 over tutulumu olan hastalarda yükselebilmektedir. Tümör belirteçlerinin yüksek olması genelde hastalığın ileri ve daha invazif olduğunu göstermektedir
Özellikle ameliyat öncesi CEA düzeyi yüksek olan hastalar hastalığın rekürrensi bakımından daha fazla risk altındadırlar
Hastalığın nadir görülmesi ve merkez başına düşen hasta sayısının çok düşük olması nedeniyle kesin bir tedavisi tanımlanmamıştır ve hangi tedavinin daha iyi olacağına dair kesin kanıtlar mevcut değildir. Cerrahi olarak daha çok yapılan debulking’tir. Hastalarda mümkün olduğu kadar mukus ve tümör künt diseksiyonla çıkartılıp sağ hemikolektomi, histerektomi ve bilateral ooferektomi eklenebilir. Bu tedavi sonrası hastalarda nüks görülür ve bu aradaki süre hastadan hastaya değişir. Hastalar uzun süre asemptomatik kalabilir. Bu hastalar tekrar laparotomiye ihtiyaç duyarlar ve her laparotomide cerrahi tedavinin etkinliği azalır. Alternatif bir cerrahi yöntem olarak Sugarbaker peritonektomi yöntemlerini önermektedir
Bu yöntemde parietal periton ve abdominal yapıların fikse olduğu bölgelerde bu organlar çıkarılmaktadır. Bu yöntemin amacı tümöral hücrelerin mümkün olduğu kadar azaltılmasıdır. Fakat bu tedavi biçiminin etkinliği konusundaki kanıtlar sınırlıdır
PMP’de cerrahi sonrası geride kalan tümör hücrelerini yok etmek için kemoterapi kullanılması önerilmektedir. Müsinöz tümörler yavaş çoğalan tümörler olduğundan ve kemoterapötik ajanların periton içine geçişi sınırlı olduğundan sistemik kemoterapinin etkisi sınırlıdır. İntraabdominal tümörlerde periton içine verilen kemoterapinin etkisi gösterildiğinden PMP’de de İK uygulamaları vardır. Genelde kullanılan yöntem ameliyatta mitomisin C, ameliyat sonrası 4-5 gün ise 5FU verilmesidir
İK’nin PMP’de etkinliği hakkında yapılmış kontrollü bir çalışma olmamasına rağmen cerrahi ve İK beraber kullanıldığında hastaların hastalıksız yaşam süresinin 10 yılı aşabildiği gösterilmiştir
Deraco ve ark. yaptıkları faz II çalışmada cerrahi olarak peritonektomi yapılıp İK verilen hastalarda yaşam süresinin uzadığı ve lokal olarak hastalık kontrolünün daha iyi sağlandığını göstermişlerdir. Biz de tedaviyi kabul eden erkek hastamızda intraperitoneal kemoterapiyi tercih etik. Çok geniş bir alana radyoterapi verilmesinin hastaya ciddi yan etkileri olacağından ve tüm periton yüzeyini tutan yaygın bir hastalık olduğundan PMP’de radyoterapi kullanılmamaktadır.
Nadir görülen PMP’nin tanısı günümüzde radyolojik ve sitolojik yöntemlerle kolaylıkla konulabilmektedir. Artık hastalar ön tanıyla ameliyata alınabildiğinden cerrah ameliyata daha hazırlıklı girebilmekte ve intraperitoneal kemoterapi ameliyat esnasında daha rahat uygulanabilmektedir. Böylece hastalarda ilk nüks daha ileriye çekilerek hastaların yaşam süresi uzatılmakta ve hastalara daha uzun süre bir hastalıksız yaşam sunulmaktadır.
Pseudomyxoma peritonei ( PMP ), bol miktarda müsin veya jelatinimsi asit üreten kanserli hücrelerin (müsinöz adenokarsinom ) neden olduğu klinik bir durumdur . Tümörler dokularda fibrozise neden olur ve sindirimi veya organ fonksiyonlarını engeller ve tedavi edilmezse ürettikleri tümörler ve müsin karın boşluğunu doldurur. Bu, organların sıkışmasına neden olacak ve kolonun , ince bağırsağın, midenin veya diğer organların işlevini bozacaktır . Çoğu durumda tedaviyle prognoz iyimserdir, ancak hastalık tedavi edilmezse öldürücüdür; kaşeksi , bağırsak tıkanıklığı veya diğer komplikasyon türleri nedeniyle ölüm meydana gelir.

Bu hastalığa çoğunlukla apendiks primer kanseri ( apendiks kanseri ) neden olur; Yumurtalıktaki müsinöz tümörler de suçlanmıştır, ancak çoğu durumda yumurtalık tutulumunun apendiks veya başka bir gastrointestinal kaynaktan metastaz olması tercih edilir . Hastalık tipik olarak düşük veya yüksek dereceli ( taşlı yüzük hücreleriyle birlikte) olarak sınıflandırılır . Hastalık düşük dereceli histolojik özelliklerle ortaya çıktığında kanser nadiren lenfatik sistem veya kan dolaşımı yoluyla yayılır .
Psödomiksoma peritonei’nin belirti ve semptomları arasında karın veya pelvik ağrı ve/veya şişkinlik, şişkinlik, sindirim bozuklukları, kilo değişiklikleri, çevre artışı ve kısırlık sayılabilir .
Pseudomyxoma peritonei (PMP, sin .: jelatinöz karsinom , jelatinöz karsinom , jelatinöz göbek ), tüm intraperitoneal alanda (karın boşluğu) az sayıda tümör hücresi içeren büyük bir mukus oluşumudur . Periton ve omentumda tümör oluşumu ile birlikte, sonunda tüm karın boşluğunu dolduran büyük miktarlarda mukus (müsinöz) asit (assit) ile birlikte görülen, çok yavaş ilerleyen bir hastalıktır .
Psödomiksoma peritonei çok nadirdir. Yaklaşık 5.000 laparotomiden (karın kesileri) yalnızca birinde bulunur . Tıp literatüründe yılda 1,4 milyon kişi başına yaklaşık bir hastalığın görülme sıklığı rapor edilmektedir.
Sebep
Primer tümörün, MUC2 eksprese eden goblet hücrelerinden ve en yaygın olarak apendiksteki bu hücrelerden ortaya çıktığı görülmektedir. K-Ras ve p53 genleri onkogenezde rol oynayabilir. Bir dizi durumla teşhis edilebilir. Bu vakaların çoğunluğu apendiks karsinomları ile ilişkili olsa da, yaygın peritoneal adenomüsinoz (DPAM), peritoneal karsinomlar, çeşitli müsinöz tümörler (müsinöz adenokarsinom, müsinöz kistadenom ve müsinöz kistadenokarsinom) dahil olmak üzere başka durumlar da bulunabilir. diğer hastalık durumları gibi. Bildirilen diğer birincil bölgeler arasında kolon , rektum , mide , safra kesesi , safra kanalları , ince bağırsak , idrar kesesi , akciğer , meme , fallop tüpleri ve pankreas yer almaktadır .
Bazen peritonun jelatinöz hastalığı veya peritonun jelatinimsi asiti olarak da adlandırılan Pseudomyxoma peritonei , ilk kez 1842’de Karel Rokitansky tarafından tanımlanan nadir bir hastalıktır .
Teşhis
Bu hastalık sıklıkla, örneğin fıtık onarımı gibi diğer durumlar için yapılan ameliyatlar sırasında keşfedilir ve bunun ardından deneyimli bir patolog tanıyı doğrulayabilir. İleri aşamalar, karın bölgesinde elle hissedilen tümörler veya karnın şişkinliği olarak ortaya çıkabilir (“jöleli göbek” bazen bu durum için argo bir terim olarak kullanılır). Bu hastalığın nadir görülmesi nedeniyle, mide bağırsak kanseri cerrahından uygun tedavinin alınabilmesi için doğru tanının alınması önemlidir. Teşhis testleri BT taramalarını, laparoskopi yoluyla elde edilen doku örneklerinin incelenmesini ve tümör belirteçlerinin değerlendirilmesini içerebilir. Çoğu durumda kolonoskopi tanı aracı olarak uygun değildir çünkü çoğu durumda apendiks kanseri karın boşluğunu istila eder ancak kolonu istila etmez (ancak kolonun içinde yayılım zaman zaman rapor edilir). PET taramaları yüksek dereceli müsinöz adenokarsinomu değerlendirmek için kullanılabilir, ancak bu test düşük dereceli tümörleri tespit etmede güvenilir değildir çünkü bunlar taramalarda ortaya çıkan boyayı almazlar. Hastalık takibi için yeni MRI prosedürleri geliştirilmektedir, ancak standart MRI’lar genellikle bir teşhis aracı olarak kullanılmamaktadır. Tanı patoloji ile doğrulanır.
Bu bir klinik sendromdur, yani. H. Bunun arkasında birçok hastalık gizlenebilir. İntraperitoneal müsinöz neoplazmın rüptürü , sızıntısı ve metastazı , psödomiksoma peritonei’nin nedeni olarak kabul edilir . Tümörün kökeni yıllardır tartışılıyor; apendiks ve yumurtalık tartışılıyor. Bununla birlikte, vermiform apendiks mukoseli veya yumurtalıkların psödomüsin kistomaları gibi bu organların iyi huylu hastalıkları da dikkate alınmaktadır.
En sık görülen semptomlar karın şişliği ve ağrıdır. Diğer olası semptomlar arasında mide bulantısı, kusma, idrar yolu sorunları , yorgunluk ve skrotum veya kasık kanalında doku kitleleri yer alır . Sonuçta içi jöle ile dolu kasık fıtıkları da gelişebilir. Mukoza kitleleri büyük miktarlarda mevcutsa diyafram yukarı doğru itilir ve nefes almayı zorlaştırır.
Sonografi, karın boşluğu boyunca ve bağırsak ansları arasında karakteristik, hassas, çizgili reflekslerin gömülü olduğu yankısız, intraperitoneal, mukus kitlesini ortaya çıkarır. Jöle hareketli ve deforme olabilir ancak klasik asitten daha yavaş reaksiyona girer. Viskozite nedeniyle grotesk, tümör benzeri şekiller ortaya çıkar. Bilgisayarlı tomografi psödomiksomanın boyutunu gösterir. Büyüklüğüne bağlı olarak, kolon ve gastroskopi gibi mide veya kalın bağırsağın ek endoskopik muayeneleri, ürolojik muayeneler veya kalp ve akciğer muayeneleri ile kan örnekleri gerekli olabilir. En önemli tanı özelliği karın boşluğunda hücre dışı mukus üretimidir.
Semptomlar spesifik değildir. Karın şişliği, psödo-apandiküler ağrı, semptomatik kasık fıtığı, spesifik olmayan bağırsak bozuklukları, tesadüfi keşif vb. Çoğu zaman hastalar, genel durumlarında bir değişiklik olmadan, kademeli olarak başlayan karın şişkinliği veya karın ağrısı nedeniyle başvururlar. Daha nadiren bulantı veya kusma da görülebilir .
Taramalarda sıklıkla geç konulan tanıdan şüphelenilebilir.
Tümör belirteçleri ACE ve CA 19.9 bazen yükselir ve prognostik katkıları açıkça gösterilmese de nüksetme taramasında faydalıdırlar
Delinme sırasında, tahliyesi çok zor olan, protein bakımından zengin (eksüdatif sıvı) çok yoğun bir sıvı bulacağız. CT veya ultrasonda psödomiksoma çoğunlukla septalıdır. Karaciğerde ve/veya dalakta hastalığa işaret eden çentikler gözlenir.
Hastalığın ilerlemesi çoğunlukla tahliyeden sonra tekrarlamadır. Lenf düğümü veya uzak metastazlar istisnai kalır.
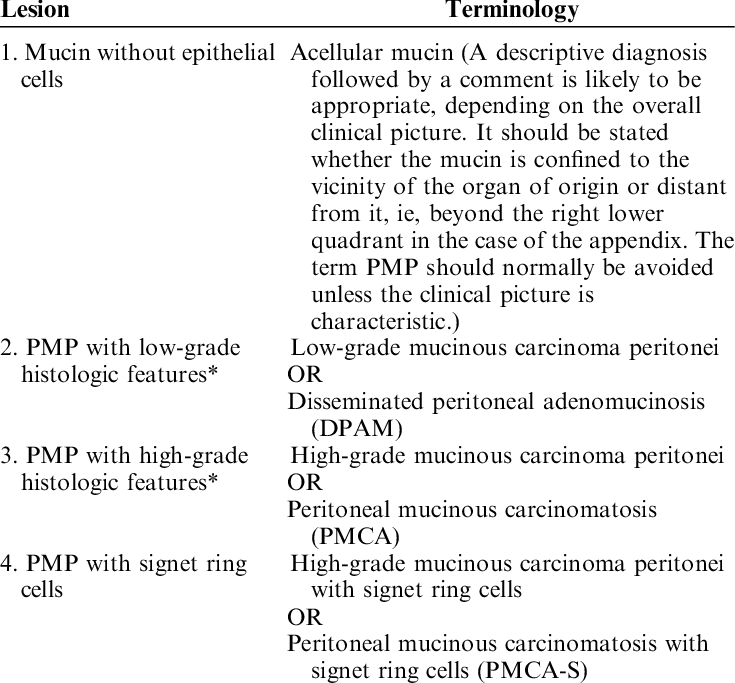
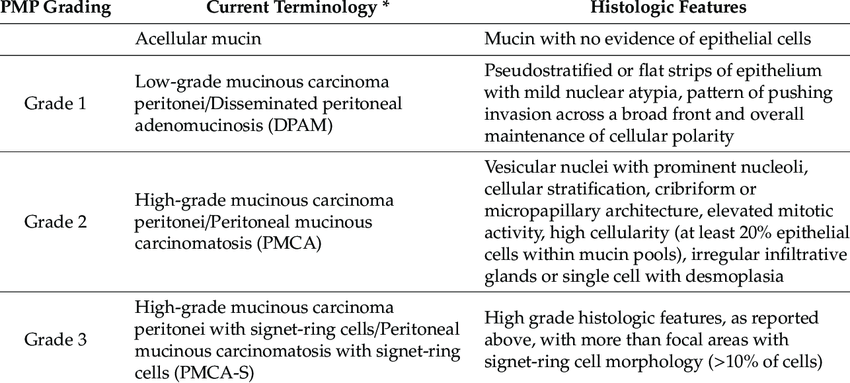
Sınıflandırma
Psödomiksoma peritonei’nin histopatolojik sınıflandırmasına ilişkin önemli tartışmalar vardır. 1995 yılında Ronnett ve ark. psödomiksoma peritonei vakalarını iki tanısal kategoriye ayırmayı önerdiler: adenom (yaygın peritoneal adenomüsinoz, DPAM) veya karsinom (peritoneal müsinöz karsinomatoz, PMCA) ve üçüncü bir kategorinin ara özelliklere sahip vakalar için ayrılması. Bu sınıflandırma sisteminde, DPAM vakaları, çok az sitolojik atipi veya mitotik aktiviteye sahip, az miktarda basit ila fokal proliferatif müsinöz epitel içeren bol miktarda hücre dışı müsin içeren peritoneal lezyonlarla karakterize edildi (başka bir deyişle, çoğu hücre oldukça normal görünüyordu ve mitoz kanıtı yoktu). bu, ilişkili apendiks müsinöz adenomu olsun ya da olmasın, hücrelerin hızla bölündüğünü gösterir. PMCA vakaları, ilişkili bir primer müsinöz adenokarsinom olsun veya olmasın, karsinomun mimari ve sitolojik özelliklerine (düzensiz hücreler, hücrelerin hızla bölündüğüne dair kanıtlar ve diğer kriterler) sahip, daha bol müsinöz epitelden oluşan peritoneal lezyonlarla karakterize edildi.
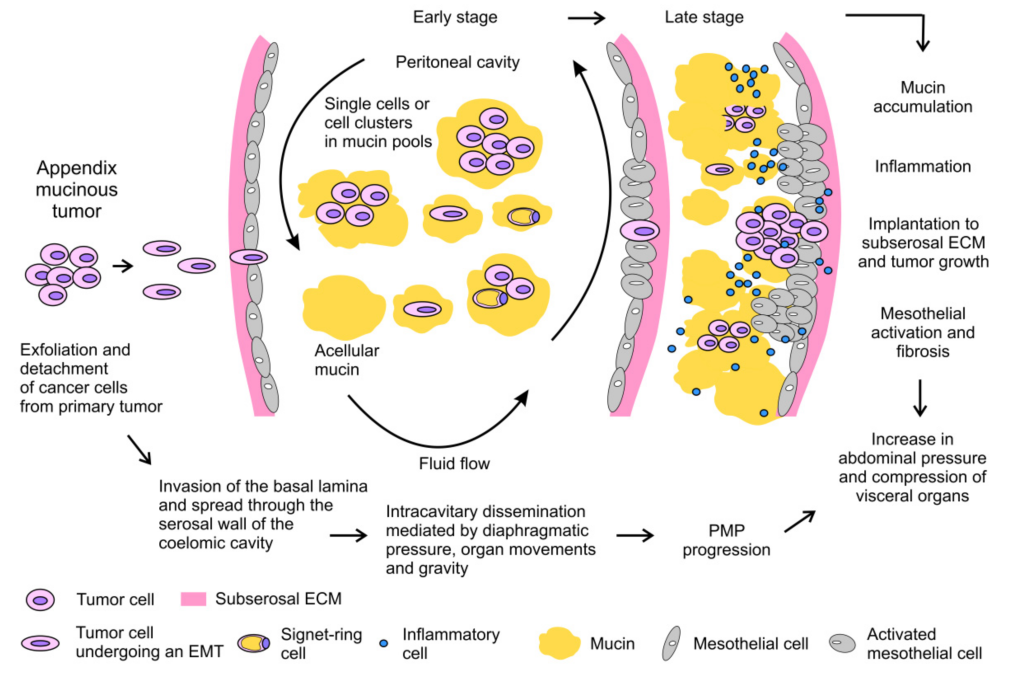
Bradley ve diğerleri. (2007) , düşük dereceli özelliklere sahip (DPAM gibi) sık görülen vakalar için malign olmayan terimlerin (adenom) kullanılmaya devam edilmesinin yanıltıcı olduğunu, çünkü psödomiksoma peritonei’nin peritonun istilasından kaynaklanan bir hastalık durumu olduğunu ileri sürmüştür. kontrolsüz büyüme gösteren hücreler tarafından karın boşluğu. Bradley, adenomun tanım gereği apendiks mukozasıyla sınırlı bir tümör olduğunu ve muskularis mukozanın ötesinde hiçbir invazyon kanıtı olmadığını belirtmektedir.
Müsinöz adenokarsinom terimi, patoloğun hastalık sınıflandırması için kullandığı referans materyale bağlı olarak farklı bağlamlarda kullanılır. Örneğin, yüksek dereceli özellikler, istilacı bezler ve/veya taşlı yüzük hücreleri ile karakterize edilen neoplazmalar, patoloji literatüründe adenokarsinom olarak adlandırılır. Bununla birlikte, bazı patologlar (örn., Odze ve Goldblum, Cerrahi Patoloji of the GI Tract, Liver, Biliary Tract and Pancreas , 2. baskı), müsinöz adenokarsinom terimini, düşük dereceli, iyi diferansiye, eksik tümörlere atıfta bulunurken kullanırlar. yüksek dereceli özellikler. Düşük dereceli müsinöz adenokarsinom, Amerikan Kanser Ortak Komitesi ve Dünya Sağlık Örgütü tarafından kullanılır ve neredeyse veya tamamen DPAM tanımıyla eşanlamlıdır. Düşük dereceli müsinöz adenokarsinom için hastalık “iyi huylu” olarak adlandırılabilir çünkü tümörler dokuya derinlemesine yayılmaz ve nadiren organ parankimine metastaz yapmaz; bu adlandırma meslekten olmayan kişiler için yanıltıcı ve kafa karıştırıcı olabilir çünkü psödomiksoma peritonei zararsız bir durum değildir ve tedavi edilmezse ölümcül olabilir. Yüksek dereceli veya az farklılaşmış müsinöz adenokarsinom genel olarak daha kötü bir prognoza sahiptir, ancak ısıtmalı intraperitoneal kemoterapi (HIPEC) ile cerrahi tedavi umut verici sonuçlar vermektedir
İmmünohistokimyasal özellikler:
SATB2, CK20, CDX2 ve mCEA’nın yaygın ifadesi
Bazen düzensiz CK7; negatif PAX8
Yüksek dereceli neoplazmalar DPC4 kaybı (%10) gösterebilir
Fizyopatoloji
Peritonun jelatinöz hastalığına, iyi huylu ve kötü huylu bir tümör sınırındaki bir tümör neden olur. Tümör çoğunlukla bağırsak eki ve yumurtalık pahasına gelişir.
Pseudomyxoma peritonei kesinlikle birincil peritoneal patoloji değildir . 1995 yılında Johns Hopkins Hastanesi’nin çok merkezli çalışmasında psödomiksomaların %95’inin apendiks kökenli olduğu belirtildi . Apendiksin submukozal adenomunun psödomiksomaya neden olduğu düşünülmektedir7 . Apendiksi tıkayan bu adenom, mukus birikmesine ve ardından genellikle çok fazla semptomatik olmayan bir yırtılmaya yol açacaktır . Jelatinimsi asitlerin varlığını buluyoruz . Düşük hücresel içerikli mukus ana yapısal unsurdur. Düşük dereceli bir adenokarsinomun histolojik özelliklerini sunar.
Belirli bir hasta için psödomiksomanın kesin sınıflandırması karmaşıktır. Aslında periton boşluğunda çeşitli dereceler bir arada bulunabilir. Ancak derecesi ne olursa olsun, bu patolojiyi hiçbir zaman iyi huylu olarak görmüyoruz çünkü evrimi az ya da çok uzun vadede her zaman öldürücüdür.
Apendiküler tümör veya apendiküler mukoselin yırtılmasından sonra müsin üreten hücreler kendilerini periton boşluğuna yerleştirir. Daha sonra müsinöz hücreler ve müsin, yapışma kapasitesinin olmaması nedeniyle periton sıvılarının yeniden emilim akımlarına ve basit yer çekimine bağlı olarak periton boşluğunda çoğalır ve birikir. Bu evrimsel tarza “yeniden dağıtım olgusu” adı verilmiştir .
Tedavi
Hem nadir görülmesi hem de sıklıkla yavaş büyüyen doğası nedeniyle tedavisi değişkendir. Tedavi, dikkatli beklemekten kitle küçültme ve sitoredüktif cerrahi ile hipertermik intraperitoneal kemoterapiye (HIPEC, aynı zamanda intraperitoneal hipertermik kemoterapi, IPHC olarak da adlandırılır) kadar uzanır .
Cerrahi
Klinik durum PMP olan müsinöz adenokarsinomun bakım standardı, PMP tedavisinde uzmanlaşmış cerrahi onkologlar tarafından gerçekleştirilen hipertermik intraperitoneal kemoterapi (HIPEC) ile birlikte sitoredüktif cerrahiyi (CRS) içerir . Bazı cerrahlar ayrıca cerrahi sitoredüksiyon ve HİPEK’e ek olarak ameliyat sonrası erken dönemde intraperitonyal kemoterapi (EPIC) de uygularlar. Hemen ameliyatın gerekli olmadığı durumlarda, hastalar BT taramaları, tümör belirteç laboratuvar testleri ve fiziksel semptomlar yoluyla izlenerek ameliyatın ne zaman ve gerekli olup olmadığı belirlenebilir. Her ne kadar bazı cerrahi prosedürler oldukça kapsamlı olsa da, hastalar ameliyattan sonra iyileşebilir ve iyileşebilir ve bu hastaların çoğunluğu verimli bir hayat yaşayabilir ve yaşayabilir.
Hastalığın etiyolojisi bilinmediğinden tedavi çoğunlukla semptomatiktir ve sıvının boşaltılmasına dayanır.
Mevcut standart tedavi, sitoredüksiyon cerrahisi ve hipertermik intraperitoneal kemoterapinin (HİPEK) kombinasyonundan oluşur. Hem düşük dereceli hem de yüksek dereceli formlarda mükemmel hayatta kalma sonuçları gözlemlenmiştir . Ne yazık ki, periton hastalığı sıklıkla çok yaygın olup, bu ağır tedavi yalnızca genel durumu mükemmel olan hastalara sunulabilmektedir. Aslında postoperatif mortalite ve morbidite riski göz ardı edilebilecek düzeyde değildir.
Uzun zamandır sınır patolojisi olarak kabul edilen psödomiksoma, bugün malign bir patoloji olarak kabul edilmelidir. Aslında, sitoredüksiyon cerrahisi ve intraperitoneal kemoterapiyi birleştiren optimal tedavinin yokluğunda, aşağı yukarı uzun vadede gelişimi öldürücüdür.
Kütle küçültmede cerrah mümkün olduğu kadar çok tümörü çıkarmaya çalışır. CRS veya sitoredüktif cerrahi, peritonun ve tümör yayılımı olduğu düşünülen komşu organların cerrahi olarak çıkarılmasını içerir . Mukus karın boşluğunun alt kısmında birikme eğiliminde olduğundan yumurtalıkların , fallop tüplerinin , uterusun ve kalın bağırsağın bazı kısımlarının çıkarılması yaygındır . Tümörün yayılmasına bağlı olarak, safra kesesi, dalak ve ince bağırsağın ve/veya midenin bazı kısımları dahil ancak bunlarla sınırlı olmamak üzere diğer organlar da çıkarılabilir . Güvenli bir şekilde çıkarılamayan organlarda ( karaciğer gibi ), cerrah tümörü yüzeyden çıkarır.
Kemoterapi
Kemoterapi (tipik olarak kemoterapötik ajan Mitomisin C kullanılarak ), sitoredüktif cerrahiden (kalan mikroskobik kanserli tümörleri ve serbest yüzen hücreleri öldürmek için tüm görünür hastalıkları ortadan kaldıran cerrahi) sonra doğrudan karın boşluğuna verilebilir. Isıtılmış kemoterapi (HİPEK), ameliyatın son adımı olarak karın boşluğu boyunca bir veya iki saat boyunca perfüze edilir veya erken olarak bilinen ameliyattan sonraki bir ila beş gün boyunca kimyasalların dolaşımına ve/veya drenajına izin verecek portlar yerleştirilir. ameliyat sonrası intraperitoneal kemoterapi (EPIC). EPIC, ameliyattan sonraki birkaç ay boyunca birden fazla döngü halinde verilebilir.
Sistemik kemoterapi ek veya adjuvan tedavi olarak uygulanabilir . Kolorektal kanser hastaları için geliştirilen yeni kemoterapilerin artan kullanılabilirliği nedeniyle, bazı hastalarda sistemik kemoterapi ile tümör büyümesinde stabilite elde edilmiştir. Sistemik kemoterapi genellikle ilerlemiş hastalığı, tekrarlayan hastalığı veya lenf düğümlerine veya uzak bölgelere yayılmış hastalığı olan hastalar için kullanılır.
Bu hastalık ameliyat ve kemoterapi sonrasında tekrarlayabilir. Hastaları hastalığın ilerlemesi açısından izlemek için ameliyat sonrası periyodik BT taramaları ve tümör belirteç laboratuvar testleri kullanılır.